

فروكتوز
فروكتوز نوعي قند ساده است كه 50٪ قند سفره (ساكارز) را تشكيل مي دهد.
قند ميز همچنين از گلوكز تشكيل شده است كه منبع اصلي انرژي سلولهاي بدن شما است.
با اين وجود ، فروكتوز قبل از استفاده توسط بدن ، بايد توسط كبد به گلوكز تبديل شود.
همچنين در انواع شيرين كننده هاي شيرين مانند شربت ذرت با فروكتوز بالا و شربت گون وجود دارد. اگر محصولي قند اضافه شده را به عنوان يكي از اصلي ترين مواد تشكيل دهنده خود ذكر كرده است ، مي توانيد مطمئن باشيد كه از نظر فروكتوز سرشار است.
قبل از توليد انبوه شكر تصفيه شده ، انسان بندرت آن را در مقادير زياد مصرف مي كرد. در حالي كه برخي از ميوه ها و سبزيجات شيرين حاوي فروكتوز هستند ، اما مقادير نسبتاً كمي را تأمين مي كنند.
بعضي از افراد تمام فروكتوزهايي را كه مي خورند جذب نمي كنند. اين وضعيت به عنوان سو mala جذب فروكتوز شناخته مي شود ، كه با گاز بيش از حد و ناراحتي گوارشي مشخص مي شود .
در كساني كه سو mala جذب فروكتوز دارند ، فروكتوز به عنوان يك كربوهيدرات قابل تخمير عمل مي كند و به عنوان FODMAP طبقه بندي مي شود.
برخلاف گلوكز ، فروكتوز باعث افزايش كم سطح قند خون مي شود. بنابراين ، برخي از متخصصان بهداشت ، فروكتوز را به عنوان يك شيرين كننده “ايمن” براي افراد مبتلا به ديابت نوع 2 توصيه مي كنند .
با اين حال ، ديگران نگران هستند كه مصرف بيش از حد فروكتوز ممكن است به چندين اختلال متابوليك كمك كند. اين نگراني ها در فصل بعدي مورد بحث قرار گرفته است.
چرا فروكتوز براي شما مضر است؟
گلوكز و فروكتوز توسط بدن بسيار متفاوت متابوليزه مي شوند.
در حالي كه هر سلول در بدن مي تواند از گلوكز استفاده كند ، كبد تنها عضوي است كه مي تواند فروكتوز را به مقدار قابل توجهي متابوليزه كند.
هنگامي كه افراد از رژيم هاي غذايي با كالري زياد و فروكتوز استفاده مي كنند ، كبد بيش از حد بار مي شود و شروع به تبديل فروكتوز به چربي مي كند.
بسياري از دانشمندان معتقدند كه مصرف بيش از حد فروكتوز مي تواند عامل اصلي بسياري از جدي ترين بيماري هاي امروزي باشد. اين موارد شامل چاقي ، ديابت نوع II ، بيماري قلبي و حتي سرطان است.
با اين حال ، مدارك انساني بيشتري لازم است. محققان در مورد ميزان فروكتوز در بروز اين اختلالات بحث مي كنند.
در حالي كه فروكتوز بيش از حد بدون شك ناسالم است ، اما اثرات آن بر سلامتي بحث برانگيز است.
با اين وجود ، مدارك قابل توجهي وجود دارد كه نگراني ها را توجيه مي كند.
خوردن مقدار زيادي فروكتوز به صورت قندهاي اضافه شده ممكن است:
تركيب چربي خون را مختل كنيد. فروكتوز ممكن است سطح كلسترول VLDL را افزايش دهد ، كه منجر به تجمع چربي در اطراف اندام ها و بيماري قلبي بالقوه شود .
سطح خون اسيد اوريك را افزايش دهيد ، منجر به نقرس و فشار خون بالا مي شود .
باعث رسوب چربي در كبد مي شود و به طور بالقوه منجر به بيماري كبد چرب غير الكلي مي شود .
ايجاد مقاومت به انسولين ، كه مي تواند منجر به چاقي و ديابت نوع II شود.
فروكتوز به اندازه گلوكز اشتها را سركوب نمي كند. در نتيجه ، ممكن است باعث پرخوري شود .
مصرف بيش از حد فروكتوز ممكن است باعث مقاومت در برابر لپتين ، اختلال در تنظيم چربي بدن و كمك به چاقي شود .
توجه داشته باشيد كه همه اين موارد فراتر از سايه ترديد در مطالعات كنترل شده اثبات نشده است. با اين حال ، شواهد هنوز وجود دارد و مطالعات بيشتر در سالها و دهه هاي آينده تصوير واضح تري ترسيم مي كنند.
فروكتوز از قندهاي اضافه شده براي شما مضر است ، ميوه مضر نيست.مهم است كه بدانيم همه اينها در ميوه كامل صدق نمي كند.
ميوه ها فقط كيسه هاي آبكي فروكتوز نيستند ، بلكه غذاهاي واقعي با تراكم كالري كم و فيبر زيادي هستند.
خوردن بيش از حد آنها سخت است و براي رسيدن به سطوح مضر فروكتوز مجبوريد مقادير بسيار زيادي بخوريد. به طور كلي ، ميوه در مقايسه با قندهاي اضافه شده ، منبع جزئي فروكتوز در رژيم غذايي است.
اثرات مضر فروكتوز در رژيم غذايي غربي حاوي كالري اضافي و قندهاي اضافي اعمال مي شود. اين ماده براي قندهاي طبيعي موجود در ميوه ها و سبزيجات كاربرد ندارد.
فرمول شيميايي
Formula: C6H12O6
Molar mass: 180.16 g/mol
Melting point: 103 °C
Density: 1.69 g/cm³
IUPAC ID: Fructose
Soluble in: Water
خريد فروكتوز
مشتريان ارجمند اگر نياز به خريد فروكتوز داريد مي توانيد جهت دريافت ليست قيمت با شماره هاي ماينو لب در تماس باشيد تا همكاران ما شما را در خريد اين محصول ياري فرمايند.










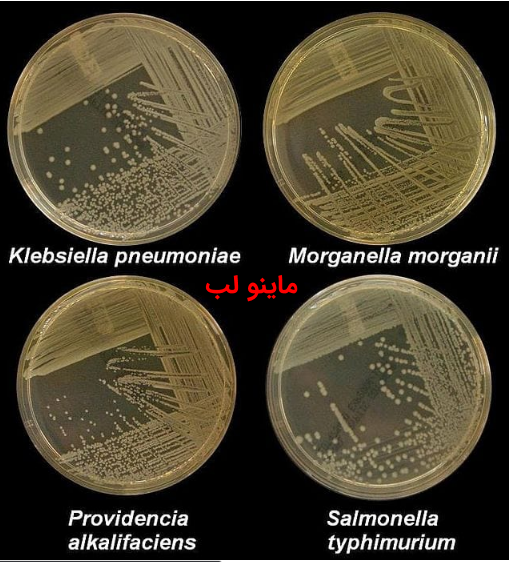 محيط كشت نوترينت آگار
محيط كشت نوترينت آگار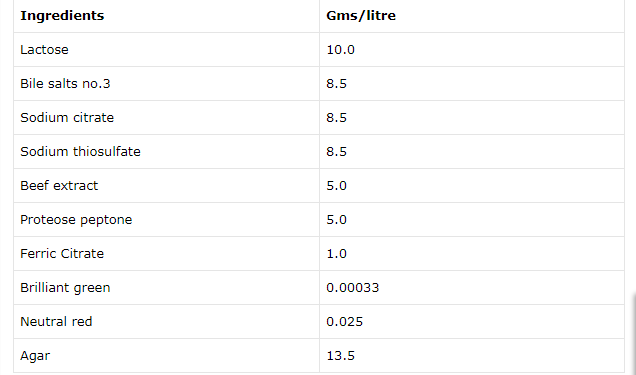 محيط سالمونلا شيگلا چيست؟
محيط سالمونلا شيگلا چيست؟ محيط كشت XLD
محيط كشت XLD محيط كشت TSA چيست
محيط كشت TSA چيست محيط كشت MHA چيست
محيط كشت MHA چيست محيط كشت مك كانكي چيست
محيط كشت مك كانكي چيست محيط كشت of چيست
محيط كشت of چيست محيط كشت بلاد آگار چيست
محيط كشت بلاد آگار چيست